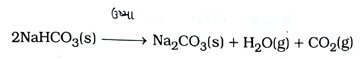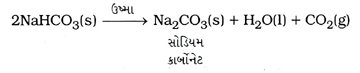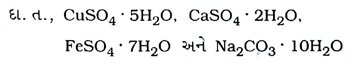Gujarat Board | Class 10Th | Chemistry | Model Question Paper & Solution | Chapter – 2 Acids, Bases and Salts (ઍસિડ, બેઇઝ અને ક્ષાર)
પ્રકરણસાર
- ઍસિડ (Acid) : તે સ્વાદે ખાટા હોય છે. તે ભૂરા લિટમસપેપરને લાલ કરે છે. તે H+(aq) આયન મુક્ત કરે છે. તેના pHનું મૂલ્ય 7 કરતાં ઓછું હોય છે, ઍસિડિક ગુણ માટે H+(aq) આયન જવાબદાર છે.
- બેઇઝ (Base) : તે સ્વાદે તૂરા હોય છે. તે લાલ લિટમસપેપરને ભૂર કરે છે. તે OH–(aq) આયન મુક્ત કરે છે. તેના pHનું મૂલ્ય 7 કરતાં વધુ હોય છે. બેઝિક ગુણ માટે OH– (aq) આયન જવાબદાર છે.
- સૂચક (Indicator) : તે ઍસિડ અને બેઇઝની હાજરીમાં રંગપરિવર્તન કરે છે અથવા ઍસિડ કે બેઇઝની હાજરીમાં વાસ બદલે છે.
- કૃત્રિમ સૂચકો : મિથાઇલ ઑરેન્જ અને ફિનોલ્ફથેલિન
- કુદરતી સૂચકો (Indicators) : લાલ કોબીજનાં પાન, હળદર, વેનિલા, ડુંગળી
- ઍસિડ ધાતુ સાથે પ્રક્રિયા કરીને હાઇડ્રોજન વાયુ ઉત્પન્ન કરે છે અને અનુરૂપ ક્ષાર (Salt) આપે છે. જ્યારે બેઇઝ ધાતુ સાથે પ્રક્રિયા કરીને હાઇડ્રોજન વાયુ ઉત્પન્ન કરે છે તથા ઉત્પન્ન થતા ક્ષારનો ત્રણ આયન એ ધાતુ અને ઑક્સિજન સાથે જોડાય છે.
- ઍસિડ ધાતુ કાર્બોનેટ અથવા ધાતુ હાઇડ્રોજન કાર્બોનેટ સાથે પ્રક્રિયા કરીને અનુરૂપ ક્ષાર, કાર્બન ડાયૉક્સાઇડ વાયુ અને પાણી આપે છે.
- પાણીમાં બનાવેલા ઍસિડિક અને બેઝિક દ્રાવણો વિદ્યુતનું વહન કરે છે, કારણ કે તેઓ અનુક્રમે હાઇડ્રોજન આયન H*(aq) અને હાઇડ્રૉક્સાઇડ આયન OH– (aq) ઉત્પન્ન કરે છે.
- pH માપક્રમ (pH scale) : તે ઍસિડ અને બેઇઝની પ્રબળતા નક્કી કરવા વપરાય છે.
- ઍસિડિક દ્રાવણ : pH < 7, pOH > 7
- બેઝિક દ્રાવણ : pH > 7, pOH < 7
- તટસ્થ દ્રાવણ : pH = 7, pOH = 7
- સજીવોમાં ચયાપચયની પ્રક્રિયાઓ મહત્તમ pH સ્તરે (7.0થી 7.8ની હદમાં) થતી હોય છે.
- સાંદ્ર ઍસિડ અથવા બેઇઝનું પાણી સાથેનું મિશ્રણ અત્યંત ઉષ્માક્ષેપક પ્રક્રિયા છે.
- તટસ્થીકરણ પ્રક્રિયા (Neutralisation reaction) : પ્રક્રિયામાં ઍસિડ અને બેઇઝ વચ્ચે પ્રક્રિયા થઈ ક્ષાર અને પાણી બને તે પ્રક્રિયાને તટસ્થીકરણ કહે છે. દૈનિક જીવનમાં તેમજ ઉદ્યોગોમાં ક્ષારનો ઉપયોગ વિવિધ સ્તરે થાય છે.
- પદાર્થ (સંયોજન) અને તેના ઉપયોગો :
- વેનિલા અર્ક, ડુંગળી, લવિંગ : ઘ્રાણેન્દ્રિય સૂચક તરીકે
- મિલ્ક ઑફ મૅગ્નેશિયા : ઍન્ટાસિડ તરીકે
- સોડિયમ ક્લોરાઇડ (NaCl) : સોડિયમ હાઇડ્રૉક્સાઇડ અને બેકિંગ સોડા, ધોવાનો સોડા, બ્લીચિંગ પાઉડરની બનાવટમાં તથા દૈનિક જીવનમાં.
- સોડિયમ હાઇડ્રૉક્સાઇડ (NaOH) : સાબુ અને ડિટર્જન્ટની બનાવટમાં, પેટ્રોલિયમના શુદ્ધીકરણમાં, પ્રયોગશાળામાં.
- બ્લીચિંગ પાઉડર (CaOCl2) : વિરંજક તરીકે, જંતુનાશક તરીકે અને ઑક્સિડેશનર્કા તરીકે.
- બેકિંગ સોડા (ખાવાનો સોડા – NaHCO3) : ઍન્ટાસિડ તરીકે, ચેપનાશક તરીકે, પ્રયોગશાળામાં, ખોરાકને નરમ બનાવવા તથા સોડા-ઍસિડ અગ્નિશામક તરીકે.
- વૉશિંગ સોડા (ધોવાનો સોડા – Na2CO3) : કાચ, સાબુની બનાવટમાં, સફાઈકર્તા તરીકે, કાગળ અને કાપડ ઉદ્યોગમાં તથા પ્રયોગશાળામાં.
- પ્લાસ્ટર ઑફ પૅરિસ (CaSO4 · ½H2O) : બાંધકામ ઉદ્યોગમાં, ફ્રેક્ચરમાં, બ્લૅકબોર્ડના ચૉક, પુતળાં બનાવવાં, બીબાં બનાવવાં તથા પ્રયોગશાળામાં.
પ્રશ્નોત્તર
પ્રશ્ન 1. ઍસિડ અને બેઇઝના સામાન્ય ગુણધર્મો લખો.
ઉત્તર : ઍસિડના ગુણધર્મો : (1) ઍસિડ સ્વાદે ખાટા હોય છે. (2) તે ભીના ભૂરા લિટમસપેપરને લાલ બનાવે છે. (3) તે બેઇઝ સાથે પ્રક્રિયા કરી ક્ષાર અને પાણી બનાવે છે. (4) તે ધાતુ સાથે પ્રક્રિયા કરી H૰(g) મુક્ત કરે છે.
બેઇઝના ગુણધર્મો : (1) બેઇઝ સ્વાદે તૂરા હોય છે. (2) તે ભીના લાલ લિટમસપેપરને ભૂરું બનાવે છે. (3) તે ઍસિડ સાથે પ્રક્રિયા કરી ક્ષાર અને પાણી બનાવે છે.
પ્રશ્ન 2. સૂચક એટલે શું? ઍસિડ-બેઇઝની પરખ માટે વપરાતા સૂચકો જણાવો.
ઉત્તર : જે દ્રાવણ ઍસિડ અને બેઇઝની હાજરીમાં રંગપરિવર્તન કરે છે, તેને સૂચક કહે છે.
ઍસિડ-બેઇઝની પરખ માટે કૃત્રિમ સૂચકો – મિથાઇલ ઑરેન્જ અને ફિનોલ્ફથેલિન તથા કુદરતી સૂચકો – લિટમસપેપર, હળદર, લાલ કોબીજનાં પાન, હાઇડ્રાન્જિયા, પેટ્નિયા અને જેરાનિયમની રંગીન પાંખડીઓનો ઉપયોગ થાય છે.
વેનિલા અર્ક, ડુંગળી, લવિંગ વગેરે પદાર્થો ઍસિડ અને બેઇઝની હાજરીમાં વાસ બદલે છે, તેમને ઘ્રાણેન્દ્રિય સૂચકો કહે છે.
આ ઉપરાંત લિટમસ દ્રાવણ જે જાંબુડિયા રંગનું હોય છે, જેને લાઇકેન કે જે થેલોફાયટા વર્ગ સાથે સંબંધ ધરાવતા છોડમાંથી કાઢવામાં આવે છે, જે સૂચક તરીકે વર્તે છે.
Intext પ્રશ્નોત્તર
પ્રશ્ન 3. તમને ત્રણ કસનળી આપવામાં આવેલ છે. તેમાંની એક નિસ્યંદિત પાણી ધરાવે છે અને બાકીની બે અનુક્રમે ઍસિડિક અને બેઝિક દ્રાવણ ધરાવે છે. જો તમને માત્ર લાલ લિટમસપેપર આપેલ હોય, તો તમે દરેક કસનળીમાં રહેલા ઘટકોની ઓળખ કેવી રીતે કરશો?
ઉત્તર : સૌપ્રથમ ત્રણ સનળીને A, B અને Cથી ચિહ્નિત કરો. સનળી A, B અને Cમાં રાખેલ દ્રાવણમાંથી એક-એક ટીપું લાલ લિટમસપેપર પર નાખો. જે કસનળીના દ્રાવણનું ટીપું લાલ લિટમસપેપરને ભૂરું બનાવે છે. તે કસનળીમાં બેઇઝ હશે તેમ કહેવાય.
હવે, બાકી રહેતી બે કસનળીમાં ઍસિડ અથવા નિસ્યંદિત પાણી હશે એમ કહેવાય.
હવે, બાકી રહેતી કસનળીના દ્રાવણમાંથી એક-એક ટીપું લઈ તેમાં બેઇઝના દ્રાવણનું એક-એક ટીપું નાખો. જે કસનળીના દ્રાવણનું ટીપું બેઇઝના દ્રાવણના ટીપા સાથે મિશ્ર થઈ રંગીન બને તે ઍસિડ છે તેમ કહેવાય અને જે મિશ્રિત ટીપાના રંગમાં કોઈ ફેરફાર થાય નહિ તે નિસ્યંદિત પાણી છે એમ કહેવાય.
આ રીતે ત્રણેય કસનળીમાં રહેલાં ઘટકોની પરખ કરી શકાય.
2.1 ઍસિડ અને બેઇઝના રાસાયણિક ગુણધર્મોની સમજ
2.1.1 પ્રયોગશાળામાં ઍસિડ અને બેઇઝ
પ્રશ્ન 4. ઘ્રાણેન્દ્રિય (Olfactory) સૂચક કોને કહે છે? ઉદાહરણ આપો.
ઉત્તર : જે પદાર્થોની ઍસિડિક કે બેઝિક માધ્યમમાં વાસ બદલાય છે, તેવા પદાર્થોને ઘ્રાણેન્દ્રિય સૂચક કહે છે.
ઉદાહરણ : વેનિલા અર્ક, ડુંગળી અને લવિંગનું તેલ.
પ્રશ્ન 5. ઘ્રાણેન્દ્રિય સૂચકની મદદથી ઍસિડ અને બેઇઝની પરખ કેવી રીતે કરશો? ઉદાહરણ આપી સમજાવો.
ઉત્તર : ઍસિડ ઘ્રાણેન્દ્રિય સૂચક(પદાર્થ)ની વાસ દૂર કરતો નથી, પરંતુ બેઇઝ ઘ્રાણેન્દ્રિય સૂચક(પદાર્થ)ની વાસ દૂર કરે છે.
દા. ત., લવિંગના તેલની વાસ ધરાવતા સ્વચ્છ કપડા ઉપર મંદ HCI(ઍસિડ)નાં ટીપાંનો છંટકાવ કરી, કપડું સુંઘતાં તેમાંથી લવિંગના તેલની વાસ આવશે. જે સૂચવે છે કે, ઍસિડ એ ઘ્રાણેન્દ્રિય સૂચકની વાસ દૂર કરતો નથી.
પરંતુ લવિંગના તેલની વાસ ધરાવતા સ્વચ્છ કપડા ઉપર મંદ NaOH(બેઇઝ)નાં ટીપાંનો છંટકાવ કરી, કપડું સુંઘતાં તેમાંથી લવિંગના તેલની વાસ દૂર થશે. જે સૂચવે છે કે, બેઇઝ એ ઘ્રાણેન્દ્રિય સૂચકની વાસ દૂર કરે છે.
2.1.2 ઍસિડ અને બેઇઝ ધાતુઓ સાથે કેવી રીતે પ્રક્રિયા કરે છે?
પ્રશ્ન 6. ઝિંક ધાતુની મંદ HCl કે મંદ H2SO4 સાથેની પ્રક્રિયાથી H2 વાયુ ઉત્પન્ન થાય છે, પણ મંદ HNO3 સાથેની પ્રક્રિયાથી H2 વાયુ ઉત્પન્ન થતો નથી? કેમ?
ઉત્તર : ઝિંક ધાતુ મંદ HCl કે મંદ H2SO4 સાથે પ્રક્રિયા કરીને H2 વાયુ ઉત્પન્ન કરે છે, કારણ કે Zn ધાતુ એ H2 વાયુ કરતાં વધુ ક્રિયાશીલ હોવાથી તે મંદ HCl કે મંદ H2SO4 માંથી સરળતાથી H2 વાયુનું વિસ્થાપન કરે છે.
જેમ કે,
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
(મંદ)
Zn(s) + H2SO4(aq) → ZnSO4(aq) + H2(g)
(મંદ)
પણ મંદ HNO3ની Zn ધાતુ સાથે પ્રક્રિયાથી H2 વાયુ ઉત્પન્ન થતો નથી, કારણ કે મંદ HNO3 પ્રબળ ઑક્સિડેશનકર્તા છે. આથી તે પ્રક્રિયા દરમિયાન ઉત્પન્ન થતા H2 વાયુનું H2O માં ઑક્સિડેશન કરે છે.
પ્રશ્ન 7. ઝિંક ધાતુની મંદ હાઇડ્રોક્લોરિક ઍસિડ અને સોડિયમ હાઇડ્રૉક્સાઇડના દ્રાવણ સાથેની સમતોલિત પ્રક્રિયા લખો.
ઉત્તર :
પ્રશ્ન 8. કઈ ધાતુઓ મંદ ઍસિડ સાથે H2 વાયુ મુક્ત કરે છે અને કઈ ધાતુઓ મંદ ઍસિડ સાથે H2 વાયુ મુક્ત કરતી નથી?
ઉત્તર : જે ધાતુ હાઇડ્રોજન કરતાં વધુ સક્રિય હોય, તે ઍસિડ સાથેની પ્રક્રિયાથી હાઇડ્રોજન વાયુ મુક્ત કરશે.
2.1.3 ધાતુ કાર્બોનેટ અને ધાતુ હાઇડ્રોજન કાર્બોનેટ ઍસિડ સાથે કેવી રીતે પ્રક્રિયા કરે છે?
પ્રશ્ન 9. સોડિયમ કાર્બોનેટ અને સોડિયમ હાઇડ્રોજન કાર્બોનેટનું મંદ હાઇડ્રોક્લોરિક ઍસિડ સાથેનું સમતોલિત સમીકરણ લખો.
ઉત્તર :
પ્રશ્ન 10. કૅલ્શિયમ હાઇડ્રૉક્સાઇડના દ્રાવણમાં ઓછા પ્રમાણમાં અને વધુ પ્રમાણમાં કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરતાં કઈ નીપજો મળે છે? મળતી નીપજની પાણીમાં દ્રાવ્યતા જણાવો.
ઉત્તર : જો કૅલ્શિયમ હાઇડ્રૉક્સાઇડના દ્રાવણમાં ઓછા પ્રમાણમાં કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરવામાં આવે, તો પાણીમાં અદ્રાવ્ય
કૅલ્શિયમ કાર્બોનેટ (CaCO3 – ચૂનાનો પથ્થર) બને છે. જેથી દ્રાવણ દૂધિયું બને છે.
આ દૂધિયા દ્રાવણમાં વધુ પ્રમાણમાં કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરવામાં આવે, તો પાણીમાં દ્રાવ્ય કૅલ્શિયમ હાઇડ્રોજન કાર્બોનેટ [Ca(HCO3)2] નીપજ બનવાને લીધે દ્રાવણનો દૂધિયો રંગ દૂર થાય છે.
પ્રશ્ન 11. કૅલ્શિયમ કાર્બોનેટ કુદરતમાં ક્યા સ્વરૂપે મળે છે?
ઉત્તર : કૅલ્શિયમ કાર્બોનેટ કુદરતમાં લાઇમસ્ટૉન (ચૂનાના પથ્થર), ચાક, આરસપહાણ, પરવાળાં, શંખ વગેરે જુદાં જુદાં સ્વરૂપે મળે છે.
પ્રશ્ન 12. સોડિયમ કાર્બોનેટના જલીય દ્રાવણમાંથી વધુ પ્રમાણમાં કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરવામાં આવે, તો કઈ નીપજ મળે છે? મળતી નીપજની પાણીમાં દ્રાવ્યતા લખો. પ્રક્રિયા સમીકરણ લખો.
ઉત્તર : સોડિયમ કાર્બોનેટના જલીય દ્રાવણમાંથી વધુ પ્રમાણમાં કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરવામાં આવે, તો સોડિયમ હાઇડ્રોજન કાર્બોનેટ (NaHCO3) મળે છે.
સોડિયમ હાઇડ્રોજન કાર્બોનેટની પાણીમાં દ્રાવ્યતા ખૂબ જ ઓછી છે.
2.1.4 ઍસિડ અને બેઇઝ એકબીજા સાથે કેવી રીતે પ્રક્રિયા કરે છે?
પ્રશ્ન 13. તટસ્થીકરણ પ્રક્રિયા કોને કહે છે? બે ઉદાહરણ આપો.
ઉત્તર : જે પ્રક્રિયામાં ઍસિડ અને બેઇઝ વચ્ચે પ્રક્રિયા થઈ ક્ષાર અને પાણી બને છે, તે પ્રક્રિયાને તટસ્થીકરણ પ્રક્રિયા કહે છે.
પ્રશ્ન 14. NaOH અને ફિનોલ્ફથેલિનના મિશ્ર દ્રાવણમાં મંદ HClનાં બે ટીપાં ઉમેરતાં રંગમાં શું પરિવર્તન થાય છે? આ રંગપરિવર્તન માટેનું કારણ જણાવો.
ઉત્તર : NaOH અને ફિનોલ્ફથેલિનના મિશ્ર દ્રાવણનો રંગ ગુલાબી છે. જો તેમાં મંદ HClનાં બે ટીપાં ઉમેરવામાં આવે, તો દ્રાવણનો ગુલાબી રંગ દૂર થાય છે.
આ રંગપરિવર્તન થવાનું કારણ તટસ્થીકરણ પ્રક્રિયા છે. જેમાં ઍસિડ દ્વારા બેઇઝ(NaOH)ની અસર નાબૂદ થાય છે.
2.1.5 ધાત્વીય ઑક્સાઇડની ઍસિડ સાથેની પ્રક્રિયા
પ્રશ્ન 15. કૉપર ઑક્સાઇડની મંદ હાઇડ્રોક્લોરિક ઍસિડ સાથે પ્રક્રિયા કરતાં શું બને છે? દ્રાવણના રંગમાં શો ફેર પડે છે? સમતોલિત સમીકરણ લખો.
ઉત્તર : કૉપર ઑક્સાઇડની મંદ હાઇડ્રોક્લોરિક ઍસિડ સાથે પ્રક્રિયા કરતાં કૉપર (II) ક્લોરાઇડ બને છે. પરિણામે દ્રાવણનો રંગ વાદળી-લીલો બને છે.
CuO(s) + 2HCl(aq) → CuCl2(aq) + H2O(1)
પ્રશ્ન 16. બેઝિક ઑક્સાઇડ કોને કહે છે? ધાત્વીય ઑક્સાઇડ કેવા પ્રકારના ઑક્સાઇડ છે? ઉદાહરણ આપો.
ઉત્તર : જે ઑક્સાઇડ પાણી સાથે પ્રક્રિયા કરી બેઇઝ બનાવતા હોય તેમને બેઝિક ઑક્સાઇડ કહે છે.
ધાત્વીય ઑક્સાઇડ બેઝિક ઑક્સાઇડ છે, કારણ કે તેઓ પાણી સાથે પ્રક્રિયા કરી બેઇઝ બનાવે છે.
2.1.6 અધાત્વીય ઑક્સાઇડની બેઇઝ સાથેની પ્રક્રિયા
પ્રશ્ન 17, ઍસિડિક ઑક્સાઇડ કોને કહે છે? અધાત્વીય ઑક્સાઇડ કેવા પ્રકારના ઑક્સાઇડ છે? ઉદાહરણ આપો.
ઉત્તર : જે ઑક્સાઇડ પાણી સાથે પ્રક્રિયા કરી ઍસિડ બનાવતા હોય તેમને ઍસિડિક ઑક્સાઇડ કહે છે.
અધાત્વીય ઑક્સાઇડ ઍસિડિક ઑક્સાઇડ છે, કારણ કે તેઓ પાણી સાથે પ્રક્રિયા કરી ઍસિડ બનાવે છે.
Intext પ્રશ્નોત્તર
પ્રશ્ન 18. શા માટે દહીં અને ખાટા પદાર્થોને પિત્તળ તેમજ તાંબાનાં વાસણોમાં ન રાખવા જોઈએ?
ઉત્તર : દહીં અને ખાટા પદાર્થો ઍસિડ ધરાવે છે, જે પિત્તળ તેમજ તાંબાનાં વાસણો સાથે પ્રક્રિયા કરે છે અને ઝેરી પદાર્થો બનાવે છે. તે માનવશરીર માટે નુકસાનકારક હોવાથી દહીં અને તેના જેવા બીજા ખાટા પદાર્થોને પિત્તળ કે તાંબાનાં વાસણોમાં રાખવા ન જોઈએ,
પ્રશ્ન 19. સામાન્ય રીતે ધાતુની ઍસિડ સાથેની પ્રક્રિયાથી કયો વાયુ મુક્ત થાય છે? ઉદાહરણ દ્વારા સમજાવો. આ વાયુની હાજરીની કસોટી તમે કેવી રીતે કરશો?
ઉત્તર : ધાતુની ઍસિડ સાથેની પ્રક્રિયાથી હાઇડ્રોજન વાયુ મુક્ત થાય છે.
દા. ત., Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g) હાઇડ્રોજન વાયુની હાજરીની કસોટી કરવા માટે સળગતી દિવાસળી કે મીણબત્તીને જ્યાં હાઇડ્રોજન વાયુ મુક્ત થાય છે, તે કસનળીના મુખ પાસે રાખતાં મુક્ત થતો હાઇડ્રોજન વાયુ ધડાકા સાથે સળગે છે.
પ્રશ્ન 20. ધાતુનું એક સંયોજન A મંદ હાઇડ્રોક્લોરિક ઍસિડ સાથે પ્રક્રિયા કરીને ઊભરા ઉત્પન્ન કરે છે. ઉત્પન્ન થતો વાયુ સળગતી મીણબત્તીને ઓલવી નાખે છે. જો ઉત્પન્ન થતાં સંયોજનો પૈકી એક કૅલ્શિયમ ક્લોરાઇડ હોય, તો પ્રક્રિયા માટે સમતોલિત રાસાયણિક સમીકરણ લખો.
ઉત્તર : ધાતુનું સંયોજન A એ CaCO3 છે
ઉદ્ભવતો વાયુ એ CO2 છે.
સમતોલિત રાસાયણિક સમીકરણ :
CaCO3(s) + 2HCl(aq) → CaCl2(aq) + CO2(g) + H2O(1)
2.2 તમામ ઍસિડ અને બેઇઝમાં શું સમાનતા છે?
પ્રશ્ન 21. આલ્કોહોલ અને ગ્લુકોઝ જેવાં સંયોજનો હાઇડ્રોજન ધરાવે છે, પરંતુ તેઓ ઍસિડની માફક વર્ગીકૃત થતા નથી, તે સાબિત કરવા માટે એક પ્રવૃત્તિ વર્ણવો.
ઉત્તર : આકૃતિ 2.3માં દર્શાવ્યા મુજબ સાધનો ગોઠવો.
હવે, દ્રાવણ તરીકે આલ્કોહોલ (ઇથેનોલ) ઉમેરો અને અવલોકન નોંધો. ત્યારબાદ આલ્કોહોલને બદલે ગ્લુકોઝનું દ્રાવણ ઉમેરો અને અવલોકન નોંધો.
અવલોકન : બંને દ્રાવણો વખતે બલ્બ પ્રકાશિત થતો નથી, જે સૂચવે છે કે, બંને દ્રાવણોમાંથી વિદ્યુતપ્રવાહ પસાર થતો નથી.
આ પ્રયોગ સૂચવે છે કે, ઇથેનોલ અને ગ્લુકોઝનું આયનીકરણ થતું નથી. પરિણામે તેમાં H+(aq) આયનો મુક્ત થતા નથી. જ્યારે ઍસિડનાં દ્રાવણોમાં H+(aq) આયનો મુક્ત થતા હોવાથી તેના દ્રાવણમાંથી વિદ્યુતપ્રવાહ પસાર થાય છે.
આમ, આલ્કોહોલ અને ગ્લુકોઝમાં હાઇડ્રોજન હોવા છતાં તેમનું ઍસિડ શ્રેણીમાં વર્ગીકરણ થતું નથી.
પ્રશ્ન 22. શા માટે નિસ્યંદિત પાણી વિદ્યુતનું વહન કરતું નથી, જ્યારે વરસાદી પાણી વિદ્યુતનું વહન કરે છે?
ઉત્તર : નિસ્યંદિત પાણી એ શુદ્ધ પાણી છે અને તે આયનો ધરાવતું નથી. જ્યારે વરસાદનું પાણી ઍસિડ જેવી અશુદ્ધિઓ ધરાવે છે, જે પાણીમાં ઓગળતા આયનો મુક્ત કરે છે.
આમ, નિસ્યંદિત પાણીમાં આયનો ન હોવાથી તેમાં વિદ્યુતનું વહન કરતું નથી, જ્યારે વરસાદી પાણીમાં આયનો હોવાથી તે વિદ્યુતનું વહન કરે છે.
2.2.1 ઍસિડ અથવા બેઇઝનું પાણીના દ્રાવણમાં શું થાય છે?
પ્રશ્ન 23. ઍસિડ પાણીની ગેરહાજરીમાં શા માટે ઍસિડિક વર્તણૂક દર્શાવતા નથી?
ઉત્તર : પાણીની ગેરહાજરીમાં ઍસિડ H+(aq) આયનો મુક્ત કરી શકતા નથી. ઍસિડિક વર્તણૂક માટે H+(aq) આયનો જવાબદાર છે. આમ, પાણીની ગેરહાજરીમાં ઍસિડ H+(aq) આયનો મુક્ત કરી શકતા ના હોવાથી તે ઍસિડિક વર્તણૂક દર્શાવતા નથી.
પ્રશ્ન 24. ઍસિડિક અને બેઝિક વર્તણૂક માટે જવાબદાર આયનો જણાવો. ઍસિડિક અને બેઇઝ વર્તણૂક પાણી સાથેની પ્રક્રિયા દ્વારા સમજાવો.
ઉત્તર : ઍસિડિક વર્તણૂક માટે H+(aq) આયન અથવા H3O+(aq) અને બેઝિક વર્તણૂક માટે OH– (aq) આયન જવાબદાર છે.
પ્રશ્ન 25. ( 1 ) શું બધા જ બેઇઝ પાણીમાં દ્રાવ્ય હોય છે? ( 2 ) પાણીમાં દ્રાવ્ય બેઇઝ કયા નામે ઓળખાય છે? (3) તેના ગુણધર્મો અને ઉદાહરણ આપો.
ઉત્તર : ( 1 ) ના
( 2 ) પાણીમાં દ્રાવ્ય બેઇઝ એ આલ્કલી તરીકે ઓળખાય છે.
( 3 ) ગુણધર્મો : તે સ્પર્શે સાબુ જેવા ચીકણા, સ્વાદે તૂરા અને ક્ષારીય હોય છે.
ઉદાહરણ : NaOH, KOH
પ્રશ્ન 26. મંદન પ્રક્રિયા કોને કહે છે? સમજાવો.
ઉત્તર : ઍસિડ અથવા બેઇઝને પાણી સાથે મિશ્ર કરતાં એકમ કદદીઠ આયનો(H3O+ અથવા OH–)ની સાંદ્રતામાં ઘટાડો થાય છે. આવી પ્રક્રિયાને મંદન (Dllution) કહે છે અને આવા ઍસિડ કે બેઇઝને મંદીકૃત (Diluted) ઍસિડ કે બેઇઝ કહે છે.
દા. ત., સાંદ્ર HNO3 કે H2SO4ને પાણીમાં ખૂબ જ ધીરે ધીરે સતત હલાવતા રહીને ઉમેરતાં, સાંદ્ર HNO3 કે H2SO4ની સાંદ્રતા ઘટે છે અને છેવટે દ્રાવણ મંદ બને છે.
પ્રશ્ન 27. સાંદ્ર સલ્ફ્યુરિક ઍસિડને મંદ કરતી વખતે શા માટે તેને પાણીમાં ઉમેરવામાં આવે છે?
અથવા
સાંદ્ર સલ્ફ્યુરિક ઍસિડને મંદ કરતી વખતે ઍસિડને પાણીમાં ઉમેરવો જોઈએ, નહિ કે પાણીને સાંદ્ર સલ્ફ્યુરિક ઍસિડમાં શા માટે?
ઉત્તર : સાંદ્ર સલ્ફ્યુરિક ઍસિડને મંદ કરતી વખતે જો ઍસિડમાં પાણી ઉમેરવામાં આવે, તો ઉત્પન્ન થતી ઉષ્મા મિશ્રણને બહારની તરફ ઉછાળી શકે છે અને દાઝી શકાય છે. ઘણી વખત અતિશય સ્થાનિક ઉષ્માને કારણે કાચનું પાત્ર તૂટી પણ શકે છે.
આથી ઍસિડને મંદ કરવા માટે ઍસિડમાં પાણી ઉમેરવાને બદલે ઍસિડને હંમેશાં પાણીમાં ખૂબ જ ધીરે ધીરે સતત હલાવતા રહીને ઉમેરવો જોઈએ. જેથી ઉત્પન્ન થતી ઉષ્મા સમગ્ર પાણીમાં પ્રસરી જાય. પરિણામે કોઈ હાનિ થતી નથી.
પ્રશ્ન 28. રસાયણોની બૉટલોના લેબલ પરનાં ચેતવણી ચિહ્નો દોરી, તેનો અર્થ લખો.
ઉત્તર :
Intext પ્રશ્નોત્તર
પ્રશ્ન 29. શા માટે HCl, HNO3 વગેરે જલીય દ્રાવણોમાં ઍસિડિક લક્ષણો ધરાવે છે, જ્યારે આલ્કોહોલ તેમજ ગ્લુકોઝ જેવાં સંયોજનોનાં દ્રાવણો ઍસિડિક લક્ષણો ધરાવતા નથી?
ઉત્તર : HCl, HNO3 વગેરે જલીય દ્રાવણોમાં H+(aq) આયન મુક્ત કરે છે. આથી તેઓનાં જલીય દ્રાવણો ઍસિડિક લક્ષણો ધરાવે છે.
જ્યારે આલ્કોહોલ તેમજ ગ્લુકોઝ વગેરે જલીય દ્રાવણોમાં H+(aq) આયન મુક્ત કરતા નથી. આથી તેઓનાં જલીય દ્રાવણો ઍસિડિક લક્ષણો ધરાવતાં નથી.
પ્રશ્ન 30. શા માટે ઍસિડનું જલીય દ્રાવણ વિદ્યુતનું વહન કરે છે?
ઉત્તર : ઍસિડ જ્યારે પાણીમાં ઓગળીને દ્રાવણ બનાવે છે ત્યારે ઍસિડનું આયનીકરણ થાય છે. પરિણામે ઉદ્ભવતા આયનોની હાજરીને કારણે તેમાંથી વિદ્યુતનું વહન થાય છે.
પ્રશ્ન 31. શા માટે શુષ્ક HCl વાયુ શુષ્ક લિટમસપેપરનો રંગ બદલતો નથી?
ઉત્તર : શુષ્ક HCl વાયુ એ H+(aq) આયન ઉત્પન્ન કરી શકતો નથી. આથી તે ઍસિડિક લક્ષણો ધરાવતો નથી. આથી તે શુષ્ક લિટમસપેપર પર કોઈ અસર કરતો નથી. આથી લિટમસપેપરનો રંગ બદલાતો નથી.
પ્રશ્ન 32. ઍસિડને મંદ કરતી વખતે શા માટે ઍસિડને પાણીમાં ઉમેરવાની, નહિ કે પાણીને ઍસિડમાં ઉમેરવાની ભલામણ કરવામાં આવે છે?
ઉત્તર : જુઓ ‘પ્રશ્નોત્તર વિભાગ’ના પ્રશ્ન 27નો ઉત્તર.
પ્રશ્ન 33. જ્યારે ઍસિડના દ્રાવણને મંદ કરવામાં આવે ત્યારે હાઇડ્રોનિયમ આયનો(H3O+)ની સાંદ્રતાને કેવી રીતે અસર થાય છે?
ઉત્તર : જ્યારે ઍસિડના દ્રાવણને મંદ કરવામાં આવે છે, ત્યારે એકમ કદીઠ હાઇડ્રોનિયમ આયનો(H3O+)ની સાંદ્રતામાં ઘટાડો થાય છે.
પ્રશ્ન 34. જ્યારે સોડિયમ હાઇડ્રૉક્સાઇડના દ્રાવણમાં વધુ પ્રમાણમાં બેઇઝ ઓગાળવામાં આવે ત્યારે હાઇડ્રૉક્સાઇડ આયનો(OH–)ની સાંદ્રતાને કેવી રીતે અસર થાય છે?
ઉત્તર : જ્યારે સોડિયમ હાઇડ્રૉક્સાઇડ(NaOH)ના દ્રાવણમાં વધુ પ્રમાણમાં બેઇઝ ઓગાળવામાં આવે ત્યારે એકમ કદ દીઠ હાઇડ્રૉક્સાઇડ આયનો(OH–)ની સાંદ્રતામાં વધારો થાય છે.
2.3 ઍસિડ અથવા બેઈઝ દ્રાવણો કેટલાં પ્રબળ છે?
પ્રશ્ન 35. ટૂંક નોંધ લખો : pH માપક્રમ
ઉત્તર : દ્રાવણમાં રહેલા હાઇડ્રોજન આયન(H+(aq))ની સાંદ્રતા માપવા માટેના માપક્રમને pH માપક્રમ કહે છે.
→ pHમાંp જર્મન શબ્દ ‘પોટેન્ઝ’ અર્થાત્ ‘શક્તિ’ સૂચવે છે.
→ pH માપક્રમ દ્વારા આપણે 0(ખૂબ જ ઍસિડિક)થી 14 (ખૂબ જ આલ્કલાઇન (બેઝિક)) સુધીની pHનું માપન કરી શકીએ છીએ.
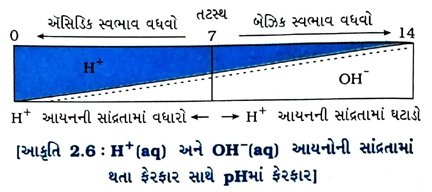
→ જેમ કે, pH માપક્રમ ૫૨ 7થી ઓછાં મૂલ્યો ઍસિડિક દ્રાવણનું સૂચન કરે છે. 7થી વધુ મૂલ્યો બેઝિક દ્રાવણનું સૂચન કરે છે. જ્યારે 7 મૂલ્ય એ તટસ્થ દ્રાવણનું સૂચન કરે છે, જે નીચેની આકૃતિ 2.6 પરથી જોઈ શકાય છે :
→ વધુમાં, જેમ pH મૂલ્ય 7થી 14 સુધી વધે છે તેમ તે દ્રાવણમાં OH આયનની સાંદ્રતામાં વધારો થાય છે અર્થાત્ આલ્કલીની પ્રબળતામાં વધારો થાય છે. આથી દ્રાવણ વધુ બેઝિક બને છે. સામાન્ય રીતે pH માપવા માટે સાર્વત્રિક સૂચક વડે સંસેચિત પેપરનો ઉપયોગ થાય છે.
→ ટૂંકમાં, જેમ હાઇડ્રોનિયમ આયન(H*(aq))ની સાંદ્રતા વધુ તેમ ઍસિડિકતા વધુ પણ pHનું મૂલ્ય ઓછું અને જેમ હાઇડ્રોનિયમ આયન(H*(aq))ની સાંદ્રતા ઓછી તેમ ઍસિડિકતા ઓછી પણ pHનું મૂલ્ય વધુ.
પ્રશ્ન 36. સાર્વત્રિક સૂચક (Universal indicator) શું છે? તેનો ઉપયોગ લખો.
ઉત્તર : સાર્વત્રિક સૂચક એ કેટલાંક સૂચકોનું મિશ્રણ છે. તેનો ઉપયોગ કરીને દ્રાવણમાંના હાઇડ્રૉક્સિલ કે હાઇડ્રૉક્સાઇડ આયનની જથ્થાત્મક માત્રા જાણી શકીએ છીએ.
દા. ત., સાર્વત્રિક સૂચક એ દ્રાવણમાંના હાઇડ્રૉક્સિલ આયનોની જુદી જુદી સાંદ્રતાએ જુદા જુદા રંગ દર્શાવે છે.
પ્રશ્ન 37. ઍસિડ અને બેઇઝની પ્રબળતા કેવી રીતે નક્કી થાય?
અથવા
નિર્બળ અને પ્રબળ ઍસિડ તથા નિર્બળ અને પ્રબળ બેઇઝ કોને કહે છે?
ઉત્તર : ઍસિડ અને બેઇઝની પ્રબળતા અનુક્રમે તેમાંથી ઉદ્ભવતા H+ આયનો અને OH– આયનોની સંખ્યા ૫૨ આધાર રાખે છે.
દા. ત., એક મોલર HCl અને એક મોલર CH3COOH એ જુદા જુદા પ્રમાણમાં H+ આયનો ઉત્પન્ન કરે છે. આથી સાંદ્રતા સમાન હોવા છતાં તેમની ઍસિડ તરીકેની પ્રબળતા જુદી જુદી હોય છે.
→ જે ઍસિડ પાણીમાં વધુ માત્રામાં H+ આયનો આપે છે, તેને પ્રબળ ઍસિડ કહે છે. દા. ત., HCl, HNO3, H2SO4 વગેરે.
→ જે ઍસિડ પાણીમાં ઓછી માત્રામાં H+ આયનો આપે છે, તેને નિર્બળ ઍસિડ કહે છે. દા. ત., HCOOH, CH3COOH, HCN વગેરે.
→ જે બેઇઝ પાણીમાં વધુ માત્રામાં OH– આયનો આપે છે, તેને પ્રબળ બેઇઝ કહે છે. દા. ત., NaOH, KOH, Ca(OH)2 વગેરે.
→ જે બેઇઝ પાણીમાં ઓછી માત્રામાં OH– આયનો આપે છે, તેને નિર્બળ બેઇઝ કહે છે. દા. ત., NH3, NH4OH વગેરે.
2.3.1 દૈનિક જીવનમાં pHનું મહત્ત્વ.
શું વનસ્પતિઓ અને પ્રાણીઓ pH પ્રત્યે સંવેદનશીલ હોય છે?
પ્રશ્ન 38. દૈનિક જીવનમાં pHનું મહત્ત્વ સમજાવો.
ઉત્તર : દૈનિક જીવનમાં pHનું મહત્ત્વ નીચે પ્રમાણે છે :
( 1 ) સજીવના અસ્તિત્વમાં pHનું મહત્ત્વ ઃ સામાન્ય રીતે માનવ-શરીરમાં થતી દેહધાર્મિક ક્રિયાઓ 7થી 7.8 pHની મર્યાદામાં થાય છે. જો આ pHમાં ફેરફાર થાય, તો જૈવિક પ્રક્રિયાઓમાં ખલેલ પહોંચે છે.
→ સામાન્ય પાણીની pH લગભગ 7.0 હોય છે, જ્યારે વરસાદી પાણીની pH લગભગ 5.6ની આસપાસ હોય છે. જે વરસાદની pH 5.6 કરતાં ઓછી હોય તેવા વરસાદને ઍસિડવર્ષા કહે છે. ઍસિડવર્ષાનું પાણી જ્યારે નદી કે તળાવ જેવાં જળાશયોમાં ભળે છે ત્યારે તેમાંના પાણીની pH ઘટે છે. પરિણામે આ જળાશયોની માછલીઓ, સૂક્ષ્મ જીવો અને જલજ વનસ્પતિઓ જેવી જલીય જીવસૃષ્ટિનું અસ્તિત્વ જોખમાય છે.
( 2 ) જમીનમાં pHનું મહત્ત્વ : વનસ્પતિના તંદુરસ્ત વિકાસ માટે વિશિષ્ટ pH મર્યાદાની જરૂરિયાત હોય છે.
→ જે જમીનની pH 6.5થી 7.3ની વચ્ચે હોય તેવી જમીનમાં છોડની વૃદ્ધિ અને વિકાસ સારો થાય છે.
→ આથી ખેડૂત ઍસિડિક જમીનને તટસ્થ કરવા જમીનમાં લાઇમ (CaO) ઉમેરે છે અને બેઝિક જમીનને તટસ્થ કરવા જમીનમાં જિપ્સમ (CaSO4 · 2H2O) ઉમેરે છે.
( 3 ) પાચનતંત્રમાં pHનું મહત્ત્વ : આપણે જાણીએ છીએ તેમ, ખોરાકના પાચનમાં જઠર અગત્યનો ભાગ ભજવે છે.
→ જઠર હાઇડ્રોક્લોરિક ઍસિડ ઉત્પન્ન કરે છે. તે જઠરને નુકસાન પહોંચાડ્યા વગર ખોરાકનું પાચન કરવામાં મદદ કરે છે. પરંતુ અપચા દરમિયાન જઠર ખૂબ વધુ માત્રામાં ઍસિડ ઉત્પન્ન કરતો હોવાથી જઠરમાં દર્દ અને બળતરા થાય છે, જેને ઍસિડિટી કહે છે.
→ ઍસિડિટીના ઉપચાર માટે બેઇઝનો ઉપયોગ કરીએ છીએ, જેને ઍન્ટાસિડ (પ્રતિઍસિડ પદાર્થ) કહે છે. તે જઠરમાં રહેલા વધારાના ઍસિડનું તટસ્થીકરણ કરે છે.
→ ઍન્ટાસિડ તરીકે મંદ બેઝિક પદાર્થો જેવા કે ખાવાનો સોડા (NaHCO3) અને મિલ્ક ઑફ મૅગ્નેશિયા (Mg(OH)2) ઉપયોગમાં લેવાય છે.
( 4 ) દાંતનું ક્ષયન (સડવું) રોકવામાં pHનું મહત્ત્વ : જ્યારે મોંના અંદરના ભાગની pH 5.5 કરતાં ઘટી જાય ત્યારે દાંતનો સડો (ક્ષયન) શરૂ થાય છે.
→ દાંતનું ઉપરનું પડ (આવરણ) કૅલ્શિયમ ફૉસ્ફેટ (Ca3(PO4)2) જેવા કઠિન પદાર્થોનું બનેલું હોય છે. તે પાણીમાં ઓગળતું નથી. પરંતુ, મોંની અંદરની pH 5.5 કરતાં ઘટી જાય ત્યારે તે પડ ખવાઈ જાય છે, જેને દાંતનું ક્ષયન થયું કહેવાય છે.
→ મોંમાં હાજર બૅક્ટેરિયા જમ્યા પછી મોંમાં બાકી રહી ગયેલા ખોરાકના ક્યો અને શર્કરાના વિઘટનથી ઍસિડ ઉત્પન્ન કરે છે, જે દાંતના ક્ષયન માટે જવાબદાર છે. આથી ખોરાક ખાધા પછી દાંત સાફ કરવા જોઈએ.
→ દાંત ચોખ્ખા કરવા માટે વપરાતી ટૂથપેસ્ટમાં સામાન્ય રીતે બેઝિક પદાર્થો હોય છે, જે વધારાના ઍસિડને તટસ્થ કરે છે. પરિણામે દાંતનો સડો અટકાવી શકાય છે.
( 5 ) મધમાખીના ડંખની અસરના ઉપચારમાં : મધમાખી જ્યારે ડંખ મારે છે ત્યારે તેનો ડંખ ઍસિડ મુક્ત કરે છે, જેને લીધે દર્દ અને સોજો આવે છે.
મધમાખીના ડંખની અસરમાં રાહત મેળવવા માટે બેકિંગ સોડા (ખાવાના સોડા) જેવા બેઝિક પદાર્થના જલીય દ્રાવણને ડંખની આસપાસના ભાગમાં લગાવવામાં આવે છે, જે ઍસિડિક ઝેરનું તટસ્થીકરણ કરે છે.
આ ઉપરાંત, કૌવચ (Nettle) નામની એક તૃણીય વનસ્પતિનાં પાંદડાના ડંખ મારતા રોમ મિથેનોઇક ઍસિડ મુક્ત કરે છે. આથી તેના સ્પર્શથી દાહક દર્દ અનુભવાય છે.
પ્રશ્ન 39. એવા કુદરતી સ્રોત જણાવો કે જેમાં ઍસિડ હોય છે.
ઉત્તર :
Intext પ્રશ્નોત્તર
પ્રશ્ન 40. તમારી પાસે બે દ્રાવણો A અને B છે. દ્રાવણ Aની PH 6 અને દ્રાવણ Bની pH 8 છે. કયા દ્રાવણમાં હાઇડ્રોજન આયનની સાંદ્રતા વધારે છે? આ પૈકી કયું દ્રાવણ ઍસિડિક અને ક્યું બેઝિક છે?
ઉત્તર : દ્રાવણ Aની pH 6 છે.
∴ તે ઍસિડિક છે. તેમાં હાઇડ્રોજન આયનની સાંદ્રતા (10–7 કરતાં) વધુ હશે. (લગભગ 10–6M જેટલી)
દ્રાવણ Bની pH 8 છે.
∴ તે બેઝિક છે. તેમાં હાઇડ્રોજન આયનની સાંદ્રતા (10-7 કરતાં) ઓછી હશે. (લગભગ 10–8M જેટલી)
પ્રશ્ન 41. H+(aq) આયનની સાંદ્રતાની દ્રાવણના સ્વભાવ પર શી અસર થાય છે?
ઉત્તર : જે દ્રાવણમાં H+(aq) આયનની સાંદ્રતા વધુ હશે, તે દ્રાવણ ઍસિડિક સ્વભાવ ધરાવશે અને જે દ્રાવણમાં H+(aq) આયનની સાંદ્રતા ઓછી હશે, તે દ્રાવણ બેઝિક સ્વભાવ ધરાવશે.
પ્રશ્ન 42. શું બેઝિક દ્રાવણો પણ H+(aq) આયનો ધરાવે છે? જો હા તો તેઓ શા માટે બેઝિક હોય છે?
ઉત્તર : હા, બેઝિક દ્રાવણો પણ H+(aq) આયનો ધરાવે છે. પરંતુ બેઝિક દ્રાવણોમાં વધુ પ્રમાણમાં OH– (aq) આયનો હોવાથી તેઓ સ્વભાવે બેઝિક હોય છે.
પ્રશ્ન 43. તમારા મત મુજબ, ખેડૂત માટીની કઈ પરિસ્થિતિમાં તેના ખેતરની માટીમાં ક્વિકલાઇમ (કૅલ્શિયમ ઑક્સાઇડ) અથવા ફોડેલો ચૂનો (કૅલ્શિયમ હાઇડ્રૉક્સાઇડ) અથવા ચાક(કૅલ્શિયમ કાર્બોનેટ)નો ઉપયોગ કરશે?
ઉત્તર : ખેતરની માટીની pH જ્યારે 6.5થી ઓછી હોય ત્યારે તે ઍસિડિક ગુણ ધરાવે છે. આ ઍસિડિક માટીને તટસ્થ કરવા માટે ખેડૂત તેમાં બેઝિક પદાર્થો જેવા કે ક્વિકલાઇમ, ફોડેલો ચૂનો કે ચાક ઉમેરે છે.
2.4 ક્ષાર વિશે વધુ (જાણકારી)
2.4.1 ક્ષાર-પરિવાર
પ્રશ્ન 44. ક્ષાર-પરિવારનો અર્થ લખો. સોડિયમ ક્ષાર, ક્લોરાઇડ ક્ષાર અને મૅગ્નેશિયમ ક્ષાર પરિવારનાં બે-બે ઉદાહરણ આપો.
ઉત્તર : એકસમાન ધન અથવા ઋણ આયનો (મૂલકો) ધરાવતા ક્ષારોને ક્ષાર-પરિવાર કહે છે.
સોડિયમ ક્ષાર-પરિવારનાં ઉદાહરણ : NaCl, Na2SO4
ક્લોરાઇડ ક્ષાર-પરિવારનાં ઉદાહરણ : NaCl, KCl
મૅગ્નેશિયમ ક્ષાર-પરિવારનાં ઉદાહરણ : MgCl2, MgSO4
2.4.2 ક્ષારની pH
પ્રશ્ન 45. તટસ્થ ક્ષાર, ઍસિડિક ક્ષાર અને બેઝિક ક્ષારનાં pH મૂલ્યો લખો.
ઉત્તર : પ્રબળ ઍસિડ અને પ્રબળ બેઇઝમાંથી બનતા તટસ્થ ક્ષારની pH 7 હોય છે.
પ્રબળ ઍસિડ અને નિર્બળ બેઇઝમાંથી બનતા ઍસિડિક ક્ષારની PH 7 કરતાં ઓછી હોય છે.
પ્રબળ બેઇઝ અને નિર્બળ ઍસિડમાંથી બનતા બેઝિક ક્ષારની PH 7 કરતાં વધુ હોય છે.
2.4.3 સામાન્ય ક્ષારમાંથી મળતાં રસાયણ
પ્રશ્ન 46. હાઇડ્રોક્લોરિક ઍસિડ અને સોડિયમ હાઇડ્રૉક્સાઇડના દ્રાવણના સંયોગીકરણથી ઉદ્ભવતા ક્ષારનું નામ અને અણુસૂત્ર લખી, તેનો ઉપયોગ અને સ્વભાવ લખો.
ઉત્તર : હાઇડ્રોક્લોરિક ઍસિડ અને સોડિયમ હાઇડ્રૉક્સાઇડના દ્રાવણના સંયોગીકરણથી સોડિયમ ક્લોરાઇડ ક્ષાર ઉદ્ભવે છે.
અણુસૂત્ર : NaCl
ઉપયોગ : ખોરાકમાં
સ્વભાવ : તટસ્થ
પ્રશ્ન 47. દરિયાના પાણીમાં ઓગળેલ ક્ષારો જણાવો.
ઉત્તર : દરિયાના પાણીમાં ઓગળેલ મુખ્ય ક્ષારો NaCl, KCl, NaBr, KBr, MgBr2 તથા NaIO3 (સોડિયમ આયોડેટ) છે.
પ્રશ્ન 48. ખનિજ ક્ષાર (રૉક સોલ્ટ) કોને કહે છે?
ઉત્તર : દરિયામાં ઓગળેલા દ્રાવ્ય ક્ષારોને ઘન ક્ષારમાં નિક્ષેપિત કરતાં મોટા સ્ફટિકો અશુદ્ધિઓને કારણે કથ્થાઈ રંગના બને છે, જેને ખનિજ ક્ષાર (રૉક સોલ્ટ) કહે છે.
પ્રશ્ન 49. ટૂંક નોંધ લખો ઃ સોડિયમ હાઇડ્રૉક્સાઇડ (NaOH)
ઉત્તર : બનાવટ ઃ સોડિયમ ક્લોરાઇડના જલીય દ્રાવણ(ક્ષારીય જળ)નું વિદ્યુતવિભાજન કરતાં ઍનોડ પાસે ક્લોરિન વાયુ મુક્ત થાય છે, જ્યારે કૅથોડ પાસે હાઇડ્રોજન વાયુ મુક્ત થાય છે તથા દ્રાવણમાં સોડિયમ હાઇડ્રૉક્સાઇડ બને છે.
2NaCl(aq) + 2H2O(1) → 2NaOH(aq) + Cl2(g) + H2(g)
આ પદ્ધતિ ક્લોર-આલ્કલી ક્રિયા તરીકે પણ ઓળખાય છે, કારણ કે તેમાં ઉત્પન્ન થતી નીપજો ફ્લોર એટલે ક્લોરિન અને આલ્કલી એટલે સોડિયમ હાઇડ્રૉક્સાઇડ છે.
આ પદ્ધતિમાં ઉદ્ભવતી ત્રણેય નીપજો ઉપયોગી છે.
ઉપયોગો : (1) ધાતુઓ પરથી ગ્રીસ દૂર કરવા માટે, (2) સાબુની બનાવટમાં, (3) પેટ્રોલિયમના શુદ્ધીકરણમાં, (4) સુતરાઉ કાપડને સુંવાળું બનાવવા માટે અને (5) પ્રયોગશાળામાં પ્રક્રિયક તરીકે.
પ્રશ્ન 50. H2 અને Cl2 ના ઉપયોગો લખો.
ઉત્તર : H2 ના ઉપયોગો : (1) બળતણ તરીકે, (2) વનસ્પતિ તેલના હાઇડ્રોજીનેશનમાં અને (૩) એમોનિયાની બનાવટમાં.
Cl2 ના ઉપયોગો : (1) જળઉપચારમાં, (2) પાણીને જંતુ રહિત બનાવવા માટે, (3) PVCની બનાવટમાં, (4) CFCsની બનાવટમાં અને (5) બ્લીચિંગ પાઉડરની બનાવટમાં.
પ્રશ્ન 51. ક્લોર-આલ્કલી ક્રિયામાં ઉદ્ભવતી ત્રણેય નીપજોની ઉપયોગિતા ચાર્ટ સ્વરૂપે લખો.
ઉત્તર :
પ્રશ્ન 52. ટૂંક નોંધ લખો : વિરંજન પાઉડર (બ્લીચિંગ પાઉડર)
અથવા
બ્લીચિંગ પાઉડરની બનાવટ અને ઉપયોગો લખો.
ઉત્તર : બનાવટ : ક્લોરિનની શુષ્ક ફોડેલા ચૂના (Slaked lime –Ca(OH)2) સાથેની પ્રક્રિયા દ્વારા વિરંજન પાઉડર બને છે.
Cl2 + Ca(OH)2 → CaOCl2 + H2O
→ વિરંજન પાઉડરને CaOCl2 દ્વારા દર્શાવાય છે, જેનું રાસાયણિક નામ કૅલ્શિયમ ઑક્સિક્લોરાઇડ છે.
વિરંજન પાઉડરનો ઉપયોગ : (1) ટૅક્સ્ટાઇલ ઉદ્યોગમાં સુતરાઉ તેમજ લિનનના વિરંજન માટે, કાગળ ઉદ્યોગમાં લાકડાના માવાના વિરંજન માટે તેમજ લૉન્ડ્રીમાં ધોયેલા કપડાના વિરંજન માટે. (2) અનેક રાસાયણિક ઉદ્યોગોમાં ઑક્સિડેશનકર્તા તરીકે. (3) પીવાના પાણીને જંતુરહિત કરવા જંતુનાશક તરીકે.
પ્રશ્ન 53. ટૂંકનોંધ લખો : બેકિંગ સોડા (ખાવાનો સોડા – NaHCO3)
અથવા
બેકિંગ સોડાની બનાવટ અને ઉપયોગો લખો
ઉત્તર : બનાવટ : સોડિયમ ક્લોરાઇડના જલીય દ્રાવણમાં CO2(g) અને NH3(g) પસાર કરતાં બેકિંગ સોડા બને છે.
સોડિયમ કાર્બોનેટના જલીય દ્રાવણમાંથી કાર્બન ડાયૉક્સાઇડ વાયુ પસાર કરતાં બેકિંગ સોડા પ્રાપ્ત થાય છે.
Na2CO3(aq) + H2O (1)+ CO2(g) → 2NaHCO3(aq)
→ બેકિંગ સોડાનું રાસાયણિક નામ સોડિયમ હાઇડ્રોજન કાર્બોનેટ અથવા સોડિયમ બાયકાર્બોનેટ છે. તે મંદ બિનક્ષારીય બેઇઝ છે.
→ ખોરાક રાંધતી વખતે તેને જ્યારે ગરમ કરવામાં આવે છે, ત્યારે નીચે મુજબ પ્રક્રિયા થાય છે અને સોડિયમ કાર્બોનેટ બને છે.
ઉપયોગો : (1) બેકિંગ સોડા અને ટાર્ટરિક ઍસિડ જેવા મંદ ખાદ્ય ઍસિડનું મિશ્રણ બેકિંગ પાઉડરની બનાવટમાં વપરાય છે, (2) તેને ગરમ કરવામાં આવે અથવા પાણી સાથે મિશ્ર કરવામાં આવે ત્યારે તેમાંથી ઉદ્ભવતા CO2 વાયુને લીધે પાઉં (Bread), કેક તથા ભજિયાં ફૂલે છે. પરિણામે તે નરમ અને પોચા બને છે. NaHCO3 + H+ → CO2 + H2O + ઍસિડનો સોડિયમ ક્ષાર (કોઈ પણ ઍસિડમાંથી), (3) ઍસિડિટીમાં રાહત મેળવવા ઍન્ટાસિડ તરીકે, (4) સોડા-ઍસિડ અગ્નિશામકમાં આગ બુઝાવવા, (5) ચેપનાશક તરીકે, (6) પ્રયોગશાળામાં પ્રક્રિયક તરીકે, (7) ઘરગથ્થુ ઉપયોગ તરીકે.
પ્રશ્ન 54. ટૂંક નોંધ લખો : ધોવાનો સોડા (વૉશિંગ સોડા – Na2CO3 · 10H2O)
અથવા
ધોવાના સોડાની બનાવટ અને ઉપયોગ જણાવો.
ઉત્તર : બનાવટ : બેકિંગ સોડાને ગરમ કરવાથી સોડિયમ કાર્બોનેટ મળે છે.
આ સોડિયમ કાર્બોનેટનું પુનઃસ્ફટિકીકરણ કરવાથી ધોવાનો સોડા મળે છે.
→ ધોવાનો સોડા એ બેઝિક ક્ષાર છે.
ઉપયોગો : (1) કાચ અને સાબુ જેવાં સંયોજનોના ઉત્પાદનમાં, (2) બોરેક્ષ જેવા સોડિયમ સંયોજનની બનાવટમાં, (૩) ઘરમાં સફાઈકર્તા તરીકે, (4) પાણીની સ્થાયી કઠિનતા દૂર કરવા માટે, (5) કાગળ અને કાપડ ઉદ્યોગમાં, (6) પ્રયોગશાળામાં પ્રક્રિયક તરીકે.
2.4.4 શું ખરેખર ક્ષારના સ્ફટિક શુષ્ક હોય છે?
પ્રશ્ન 55. સ્ફટિક જળ શું દર્શાવે છે? સ્ફટિક જળ ધરાવતા સ્ફટિકો લખો.
ઉત્તર : સ્ફટિક જળ એ ક્ષારના સ્ફટિકમય સ્વરૂપમાં પ્રત્યેક એકમ સૂત્રદીઠ રાસાયણિક રીતે જોડાયેલા પાણીના અણુઓની નિશ્ચિત સંખ્યા છે.
પ્રશ્ન 56. શુષ્ક કસનળીમાં કૉપર સલ્ફેટના સ્ફટિકને ગરમ કરતાં શા માટે તે રંગવિહીન બને છે?
ઉત્તર : કૉપર સલ્ફેટના એક એકમ સૂત્રમાં પાણીના પાંચ અણુઓ હાજર હોય છે. આ પાણીના અણુઓની હાજરીને કારણે કૉપર સલ્ફેટના સ્ફટિક ભૂરા રંગના દેખાય છે. હવે, આવા સ્ફટિકને ગરમ કરવામાં આવે, તો પાણીના અણુઓ દૂર થાય છે. પરિણામે સ્ફટિક રંગવિહીન બને છે.
પ્રશ્ન 57. ટૂંક નોંધ લખો : પ્લાસ્ટર ઑફ પૅરિસ – POP
અથવા
પ્લાસ્ટર ઑફ પૅરિસની બનાવટ અને ઉપયોગો લખો.
ઉત્તર : બનાવટ : જ્યારે જિપ્સમ(ચિરોડી)ને 373 K તાપમાને ગરમ કરવામાં આવે છે, ત્યારે તે પાણીના અણુઓ ગુમાવીને પ્લાસ્ટર ઑફ પૅરિસ બને છે.
આમ, પ્લાસ્ટર ઑફ પેરિસ (POP) એ કૅલ્શિયમ સલ્ફેટનો હેમી (અડધો) ઘઈડ્રેટ છે. જેમાં બે Ca2+ અને બે SO42- આયનો સાથે પાણીનો એક અણુ જોડાયેલો હોય છે.
પ્લાસ્ટર ઑફ પૅરિસ સફેદ પાઉડર છે અને પાણી સાથે મિશ્ર કરતાં તે સખત ધન પાર્થ જિપ્સમમાં ફેરવાય છે.
ઉપયોગો : (1) બાંધકામ ઉદ્યોગમાં તથા પ્લાસ્ટરમાં થાય છે. (2) ફ્રેક્ચર થયેલાં હાડકાંને સાચી સ્થિતિમાં ગોઠવવા માટે પ્લાસ્ટર તરીકે, (3) ાંતનાં ચોકઠાં માટેનાં બીબાં બનાવવા માટે. (4) રમકડાં અને પૂતળાં બનાવવા માટે. (5) બ્લૅક્બોર્ડ પર લખવાના ચૉક બનાવવા માટે. (6) પ્રયોગશાળામાં સાધનો અથવા પાત્રોને હવાચુસ્ત કરવા માટે તેનું પ્લાસ્ટર લગાડાય છે.
સ્વાધ્યાયના પ્રશ્નોત્તર
1. એક દ્રાવણ લાલ લિટમસને ભૂરું બનાવે છે. તેની pH લગભગ …………. હશે.
(a) 1
(b) 4
(c) 5
(d) 10
ઉત્તર : (d) 10
2. એક દ્રાવણ ઈંડાંના પીસેલા ક્વચ (કોષો) સાથે પ્રક્રિયા કરી વાયુ ઉત્પન્ન કરે છે, જે ચૂનાના પાણીને દૂધિયું બનાવે છે, તો દ્રાવણ ……. ધરાવે છે.
(a) NaCl
(b) HCl
(c) LiCl
(d) KCl
ઉત્તર : (b) HCl
3. 10 mL NaOHના દ્રાવણનું 8mL આપેલ HClના દ્રાવણ વડે સંપૂર્ણ તટસ્થીકરણ થાય છે. જો આપણે તે જ NaOHનું 20 mL દ્રાવણ લઈએ, તો તેને તટસ્થ કરવા માટે HClના દ્રાવણ(પહેલાં હતું તે જ દ્રાવણ)ની જરૂરી માત્રા ……
(a) 4 mL
(b) 8mL
(c) 12 mL
(d) 16mL
ઉત્તર : (d) 16 mL
Hint : તટસ્થીકરણ પ્રક્રિયા મુજબ, 10 mL NaOH એ 8m HClનું તટસ્થીકરણ કરે છે.
4. અપચાના ઉપચાર માટે નીચેના પૈકી કયા પ્રકારની દવાઓનો ઉપયોગ થાય છે?
(a) ઍન્ટિબાયોટિક (પ્રતિજીવી)
(b) એનાલ્જેસિક (વેદનાહર)
(c) ઍન્ટાસિડ (પ્રતિઍસિડ)
(d) ઍન્ટિસેપ્ટિક (જીવાણુનાશી)
ઉત્તર : (c) ઍન્ટાસિડ (પ્રતિઍસિડ)
5. નીચે દર્શાવેલ પ્રક્રિયાઓ માટે પહેલાં શબ્દ સમીકરણો અને ત્યારબાદ સમતોલિત સમીકરણો લખો :
(a) મંદ સલ્ફ્યુરિક ઍસિડની દાણાદાર ઝિંક સાથે પ્રક્રિયા કરતાં.
(b) મંદ હાઇડ્રોક્લોરિક ઍસિડની મૅગ્નેશિયમની પટ્ટી સાથે પ્રક્રિયા કરતાં.
(c) મંદ સલ્ફ્યુરિક ઍસિડની ઍલ્યુમિનિયમના ભૂકા સાથે પ્રક્રિયા કરતાં.
(d) મંદ હાઇડ્રોક્લોરિક ઍસિડની લોખંડના વહેર સાથે પ્રક્રિયા કરતાં.
ઉત્તર :
6. પાંચ દ્રાવણો A, B, C, D અને Eને સાર્વત્રિક સૂચક દ્વારા તપાસતાં તે અનુક્રમે 4, 1, 11, 7 અને 9 pH દર્શાવે છે, તો કયું દ્રાવણ …
(a) તટસ્થ હશે?
(b) પ્રબળ બેઝિક હશે?
(c) પ્રબળ ઍસિડિક હશે?
(d) નિર્બળ ઍસિડિક હશે?
(e) નિર્બળ બેઝિક હશે?
pHનાં મૂલ્યોને હાઇડ્રોજન આયનની સાંદ્રતાના ચડતા ક્રમમાં દર્શાવો.
ઉત્તર :
(1) ( a ) દ્રાવણ ‘D’ તટસ્થ હશે.
‘.’ તેની pH 7 છે.
( b ) દ્રાવણ‘C’– પ્રબળ બેઝિક હશે.
‘.’ તેની pH 11 (સૌથી વધુ) છે.
( C ) દ્રાવણ ‘B’ પ્રબળ ઍસિડિક હશે.
‘.’ તેની pH 1 (સૌથી ઓછી) છે.
( d ) દ્રાવણ ‘A’ નિર્બળ ઍસિડિક હશે.
‘.’ તેની pH 4 છે.
( e ) દ્રાવણ ‘E’ નિર્બળ બેઝિક હશે.
‘.’ તેની pH 9 છે.
( 2 ) pHનાં મૂલ્યોને આધારે હાઇડ્રોજન આયનની સાંદ્રતાનો ચડતો ક્રમ નીચે પ્રમાણે છે :
pH : 11 < 9<7< 4 < 1
(હાઇડ્રોજન : 10–11 < 10-9 < 10-7 < 10-4 < 10-1 આયનની
સાંદ્રતા Mમાં) ([H+] = 10-pH)
7. કસનળી A અને Bમાં સમાન લંબાઈની મૅગ્નેશિયમની પટ્ટીઓ લીધેલી છે. કસનળી Aમાં હાઇડ્રોક્લોરિક ઍસિડ (HCl) ઉમેરવામાં આવે છે અને કસનળી Bમાં ઍસિટિક ઍસિડ (CH3COOH) ઉમેરવામાં આવે છે. કઈ કસનળીમાં અતિ તીવ્ર H2(g)ના ઊભરા મળે છે? શા માટે?
ઉત્તર : હાઇડ્રોક્લોરિક ઍસિડ (HCl) એ ઍસિટિક ઍસિડ (CH3COOH) કરતાં વધુ પ્રબળ ઍસિડ હોવાથી તેનું પ્રક્રિયા દરમિયાન H+ અને Cl– આયનોમાં સંપૂર્ણ આયનીકરણ થતાં વધુ H+ આયનો ઉત્પન્ન થાય છે. આથી કસનળી Aમાં અતિ તીવ્ર H2(g)ના ઊભરા મળશે.
8. તાજા દૂધની pH 6 છે. જો તેનું દહીંમાં રૂપાંતર થાય, તો તેની pHના ફેરફાર વિશે તમે શું વિચારો છો? તમારો ઉત્તર સમજાવો.
ઉત્તર : દૂધનું જ્યારે દહીંમાં રૂપાંતર થાય છે ત્યારે લૅક્ટિક ઍસિડ બને છે. તેને લીધે pHનું મૂલ્ય ઘટે છે અને દહીં સ્વાદે ખાટું લાગે છે.
9. એક દૂધવાળો તાજા દૂધમાં ખૂબ જ અલ્પ માત્રામાં બેકિંગ સોડા ઉમેરે છે.
(a) તે તાજા દૂધની pHને 6થી થોડી બેઝિક તરફ શા માટે ફેરવે છે?
(b) શા માટે આવું દૂધ દહીં બનવા માટે વધુ સમય લે છે?
ઉત્તર : ( a ) તાજા દૂધમાં બેકિંગ સોડા ઉમેરવામાં આવે, તો pHનું મૂલ્ય 6થી વધે છે, કારણ કે બેકિંગ સોડા બેઝિક ગુણ ધરાવે છે.
(b) દૂધમાં અલ્પ માત્રામાં બેકિંગ સોડા (ખાવાનો સોડા) ઉમેરતાં દૂધ બેઝિક બને છે. તેથી દૂધમાં રહેલ લૅક્ટિક ઍસિડનું તટસ્થીકરણ થાય છે અને તેથી દૂધ દહીંમાં રૂપાંતરિત થવા માટે વધુ સમય લે છે.
10. પ્લાસ્ટર ઑફ પૅરિસને ભેજમુક્ત પાત્રમાં સંગૃહીત કરવું જોઈએ. શા માટે? સમજાવો.
ઉત્તર : પ્લાસ્ટર ઑફ પૅરિસને ભેજયુક્ત પાત્ર(વાસણ)માં સંગૃહીત કરવું જોઈએ, કારણ કે તે ભેજ સાથે પ્રક્રિયા કરી સખત ઘન પદાર્થ જિપ્સમમાં ફેરવાય છે. પરિણામે તે પ્લાસ્ટર ઑફ પૅરિસ તરીકેનો ગુણ ધરાવતો નથી.
11. ધોવાનો સોડા અને બેકિંગ સોડાના બે મહત્ત્વના ઉપયોગો આપો.
ઉત્તર : ધોવાનો સોડાના ઉપયોગો : (1) કાચ, સાબુ, કાપડ અને પેપર ઉદ્યોગમાં. (2) પાણીની સ્થાયી કઠિનતા દૂર કરવા માટે.
બેકિંગ સોડાના ઉપયોગો : (1) ઍન્ટાસિડ અને ચેપનાશક તરીકે. (2) સોડા-ઍસિડનો ઉપયોગ આગ બુઝાવવા માટે.
હેતુલક્ષી પ્રશ્નોત્તર
પ્રશ્ન 1. નીચેના પ્રશ્નોના ટૂંકમાં ઉત્તર આપો :
(1) જિપ્સમ અને પ્લાસ્ટર ઑફ પૅરિસમાં રહેલા પાણીના અણુઓનો તફાવત કેટલો હશે?
ઉત્તર : જિપ્સમમાં પાણીના 2 અણુ હોય છે, જ્યારે પ્લાસ્ટર ઑફ પૅરિસમાં પાણીનો 1/2 અણુ છે. આથી, પાણીના અણુનો તફાવત = 2 – 1/2 = 1½ હશે.
(2) સોડાલાઇમ એટલે શું? તેમાં કળીચૂનાની ભૂમિકા શું છે?
ઉત્તર : કોસ્ટિક સોડા (NaOH) અને કળીચૂના (લાઇમ – CaO)ના મિશ્રણને સોડાલાઇમ કહે છે.
તેમાં કળીચૂનાની ભૂમિકા ભેજ શોષવાની છે.
(3) અગ્નિશામક સોડા-ઍસિડ આગને કેવી રીતે બુઝાવે છે?
ઉત્તર : સોડા-ઍસિડ હવાનો સંસર્ગ બંધ કરીને આગને બુઝાવે છે.
(4) પાણી, હાઇડ્રોક્લોરિક ઍસિડ અને ઍસિટિક ઍસિડને તેમની ઍસિડિકતાના ઊતરતા ક્રમમાં ગોઠવો.
ઉત્તર : ઍસિડિકતાનો ઊતરતો ક્રમ ઃ હાઇડ્રોક્લોરિક ઍસિડ > ઍસિટિક ઍસિડ > પાણી.
(5) ક્લોર-આલ્કલી પ્રક્રિયા દરમિયાન થતી પ્રક્રિયાનું સમતોલિત સમીકરણ લખો.
ઉત્તર : 2NaCl(aq) + 2H2O(1) → 2NaOH(aq) + Cl2(g) + H2(g)
(6) મંદન પ્રક્રિયા કોને કહે છે?
ઉત્તર : ઍસિડ અથવા બેઇઝને પાણી સાથે મિશ્ર કરતાં એકમ કદદીઠ આયનોની સાંદ્રતામાં ઘટાડો થાય છે. આ પ્રક્રિયાને મંદન પ્રક્રિયા કહે છે.
(7) ઝિંકની સોડિયમ હાઇડ્રૉક્સાઇડ સાથે પ્રક્રિયા થતા મળતી નીપજનું નામ અને અણુસૂત્ર લખો.
ઉત્તર : સોડિયમ ઝિંકેટ – Na2ZnO2
(8) સામાન્ય રીતે ધાતુ અને અધાતુ તત્ત્વોના ઑક્સાઇડ કેવો ગુણ ધરાવે છે?
ઉત્તર : સામાન્ય રીતે ધાતુ તત્ત્વોના ઑક્સાઇડ બેઝિક, જ્યારે અધાતુ તત્ત્વોના ઑક્સાઇડ ઍસિડિક ગુણ ધરાવે છે.
(9) દૂધમાંથી દહીં બને ત્યારે કયો ઍસિડ ઉત્પન્ન થાય છે?
ઉત્તર : દૂધમાંથી દહીં બને ત્યારે વૅક્ટિક ઍસિડ ઉત્પન્ન થાય છે.
(10) ઍસિડિક અને બેઝિક ગુણધર્મો માટે જવાબદાર આયનો ક્યા છે?
ઉત્તર : ઍસિડિક ગુણધર્મ માટે H+(aq) આયન અને બેઝિક ગુણધર્મ માટે OH– (aq) આયન જવાબદાર છે.
(11) યૂરિયાના જલીય દ્રાવણમાંથી વિદ્યુતનું વહન થશે? શા માટે?
ઉત્તર : ના, કારણ કે યૂરિયાના જલીય દ્રાવણમાં OH– (aq) કે H3O+ આયનો મુક્ત થતા નથી.
(12) આલ્કલી પ્રબળ બેઇઝનાં બે ઉદાહરણ આપો.
ઉત્તર : NaOH અને KOH એ બે પ્રબળ આલ્કલી બેઇઝ છે.
(13) ભોજન પહેલાં અને ભોજન પછી લાળનો સ્વભાવ કેવો બને છે?
ઉત્તર : ભોજન પહેલાં લાળનો સ્વભાવ બેઝિક હોય છે, પરંતુ ભોજન પછી લાળનો સ્વભાવ ઍસિડિક બને છે.
(14) ઍસિડવર્ષા કોને કહે છે?
ઉત્તર : જે વરસાદી પાણીની pH 5.6 કરતાં ઓછી હોય તેને ઍસિડવર્ષા કહે છે.
(15) કેટલી pH મર્યાદામાં જમીનમાં છોડની વૃદ્ધિ અને વિકાસ સારો થાય છે?
ઉત્તર : જે જમીનની pH 6.5થી 7.3ની મર્યાદામાં હોય તેવી જમીનમાં છોડની વૃદ્ધિ અને વિકાસ સારો થાય છે.
(16) લાલ કીડી ચટકો ભરે છે ત્યારે આપણને બળતરા કેમ થાય છે?
ઉત્તર : લાલ કીડી ચટકો ભરે છે ત્યારે તેના દ્વારા આપણા શરીરમાં ફૉર્મિક ઍસિડ (મિથેનોઇક ઍસિડ) દાખલ થાય છે, જેને પરિણામે આપણને બળતરા થાય છે.
પ્રશ્ન 2. એક શબ્દમાં ઉત્તર આપો :
(1) કૉસ્ટિક પોટાશનું રાસાયણિક સૂત્ર લખો.
(2) ઍક્વારિજીયા એ કોનું મિશ્રણ છે?
(3) સોડા ફૅશનું સૂત્ર લખો.
(4) કયું સંયોજન ક્લોરિન સાથે પ્રક્રિયા કરીને વિરંજન પાઉડર બનાવે છે?
(5) નારંગીમાં કયો ઍસિડ હોય છે?
(6) માનવરુધિરનું pH મૂલ્ય જણાવો.
(7) સામાન્ય તાપમાને પદાર્થને વાતાવરણમાં રાખતાં તે સ્ફટિકીકરણનું પાણી મુક્ત કરે છે, જે કયા નામે ઓળખાય છે?
(8) ઍસિડમાં બેઇઝ ઉમેરવાની પ્રક્રિયા કયા નામે ઓળખાય છે?
(9) સોડિયમ, પોટૅશિયમ તત્ત્વો શેના તરીકે ઓળખાય છે?
(10) ખોરાકમાં ઉપયોગી હોય તેવા જાણીતા ક્ષારનું રાસાયણિક નામ લખો.
ઉત્તર :
(1) KOH
(2) 1 ભાગ સાંદ્ર HNO3 + 3 ભાગ સાંદ્ર HCl
(3) Na2CO3
(4) Ca(OH)2
(5) ઍસ્કોર્બિક ઍસિડ
(6) 7.36થી 7.42 (અંદાજિત 7,4)
(7) પ્રસ્ફુટન
(8) તટસ્થીકરણ પ્રક્રિયા
(9) આલ્ક્લી તત્ત્વો
(10) સોડિયમ ક્લોરાઇડ
પ્રશ્ન 3. વ્યાખ્યા આપો :
(1) ઘ્રાણેન્દ્રિય સૂચક
ઉત્તર : જે પદાર્થોની ઍસિડિક કે બેઝિક માધ્યમમાં વાસ બદલાય છે, તેવા પદાર્થોને ધ્રાબ્રેન્દ્રિય સૂચક કહે છે.
(2) તટસ્થીકરણ પ્રક્રિયા
ઉત્તર : જૈ પ્રક્રિયામાં ઍસિડ અને બેઇઝ વચ્ચે પ્રક્રિયા થઈ ક્ષાર અને પાણી બને છે, તેવી પ્રક્રિયાને તટસ્થીકરણ પ્રક્રિયા કહે છે.
(3) મંદન પ્રક્રિયા
ઉત્તર : ઍસિડ અથવા બેઇઝને પાણી સાથે મિશ્ર કરતાં એકમ કદીઠ H+ અથવા OH– આયનની સાંદ્રતામાં ઘટાડો થાય તે પ્રક્રિયાને મંદન પ્રક્રિયા કહે છે.
(4) pH માપક્રમ
ઉત્તર : દ્રાવણમાં રહેલા હાઇડ્રોજન આયનો[H†(aq)ની સાંદ્રતા માપવા માટેના માપક્રમને pH માપક્રમ કહે છે.
(5) ક્ષાર-પરિવાર
ઉત્તર : એક્સમાન ધન અથવા ઋણ આયનો ધરાવતા ક્ષારોને ક્ષાર-પરિવાર કહે છે.
(6) ખનિજ ક્ષાર (રૉક સોલ્ટ)
ઉત્તર : દરિયામાં ઓગળેલા દ્રાવ્ય ક્ષારોને ધન ક્ષારોમાં નિક્ષેપિત કરતાં મોટા સ્ફટિકો અશુદ્ધિઓને કારણે કથ્થાઈ રંગના બને છે, જેને ખનિજ ક્ષાર કહે છે.
પ્રશ્ન 4. ખાલી જગ્યા પૂરોઃ
(1) ઍસિડ અને બેઇઝ વચ્ચે તટસ્થીકરણ પ્રક્રિયા થઈ …….. અને ……. બને છે.
(2) ઍસિડિક દ્રાવણની pH …….. કરતાં ઓછી હોય છે.
(3) 4 pHવાળા જલીય દ્રાવણ કરતાં 2 pHવાળું જલીય દ્રાવણ વધુ ……. હોય છે.
(4) મિલ્ક ઑફ મૅગ્નેશિયાનો ઉપયોગ …….. તરીકે થાય છે.
(5) જિપ્સમનું આણ્વીય સૂત્ર ……. છે.
(6) છાશ ……. સ્વભાવ ધરાવે છે.
(7) હળદર એ એક …….. સૂચક છે.
(8) ………. ગ્રહનું વાતાવરણ સસ્યુટિક એસિડના કદ અને પીળાશપડતા જાનું વાદળોનું બનેલું છે.
(9) સામાન્ય રીતે pH માપવા માટે સાર્વત્રિક સૂચક સાથે ……… કાગળનો ઉપયોગ થાય છે,
ઉત્તર :
(1) ક્ષાર, પાર્ટી
(2) 7
(3) ઍસિડિક
(4) ઍસિડ
(5) CaSO4 . 2H2O
(6) એસિડિક
(7) કુદરતી
(8) શુક્ર
(9) અંતરિત(Imprenated)
પ્રશ્ન 5. નીચેનાં વિશ્વનો ખરાં છે કે ખોટાં તે જણાશે:
(1) સોડિયમ ઝિંકેટનું આણ્વીય સૂત્ર Na2Zn(OH)4 છે.
(2) ધોવાના સોડાનું જલીય દ્રાવણ ઍસિડિક સ્વભાવ ધરાવે છે.
(3) જમ્યા બાદ મોંમાં રહેલ ખોરાના ક્યોનું બૅક્ટેરિયા દ્વારા વિઘટન થઇ બેઇડ પેદા થાય છે.
(4) લોહીની pH 7થી વધુ હોય છે.
(5) નારંગીમાં સાઇટ્રિક એસિડ હોય છે.
(6) બેઇઝની રાસાયણિક પ્રક્રિયા માટે OH– (aq) આયન જવાબદાર છે.
(7) ફિનોથેલીન એ કુદરતી સૂચક છે.
(8) Ca(HCO3)2 એ પાણીમાં દ્રાવ્ય છે.
(9) Cl4O7 એ બેઝિક ઑક્સાઇડ છે.
(10) ગ્લુકોઝનું જલીય દ્રાવણ વિદ્યુતનું વહન કરતું નથી.
(11) પાણીની ઉપસ્થિતિમાં HCIમાં હાઇડ્રોજન આયનો ઉદ્ભવે છે.
(12) ઍસિડ અને બેઇઝની પાણીમાં ઓગળવાની પ્રક્રિયા ઉષ્માશોષક હોય છે.
(13) pHમાં p જર્મન શબ્દ ‘પોટેન્ડ’ સૂચવે છે.
(14) પ્રબળ ઍસિડ અને પ્રબળ બેઇઝના ક્ષાર pHના 7 મૂલ્ય સાથે તટસ્થ હોય છે.
(15) ખોરાકને ઝડપી રાંધવા માટે બેકિંગ પાઉડર વપરાય છે.
ઉત્તર :
(1) ખોટું
(2) ખોટું
(3) ખોટું
(4) ખરું
(5) ખરું
(6) ખરું
(7) ખોટું
(8) ખરું
(9) ખોટું
(10) ખરું
(11) ખરું
(12) ખોટું
(13) ખરું
(14) ખરું
(15) ખોટું
પ્રશ્ન 6. નીચેના દરેક પ્રશ્ન માટે આપેલા વિકલ્પોમાંથી સાચો વિકલ્પ પસંદ કરી ઉત્તર લખો :
1. દાંતનું ક્ષયન ક્યારે થાય છે?
A. જ્યારે મોંના અંદરના ભાગની pH 5.5 કરતાં ઓછી હોય ત્યારે
B. જ્યારે મોંના અંદરના ભાગની pH 5.5 કરતાં વધુ હોય ત્યારે
C. જ્યારે મોંના અંદરના ભાગની pH 5.5 હોય ત્યારે
D. જ્યારે મોંના અંદરના ભાગની pH 7.0 હોય ત્યારે
ઉત્તર : A. જ્યારે મોંના અંદરના ભાગની pH 5.5 કરતાં ઓછી હોય ત્યારે
2. નીચેના પૈકી કયું દ્રાવણ વધુ બેઝિક છે?
A. pH = 8.2
B. pH = 9.3
C. pH = 11.5
D. pH = 10.6
ઉત્તર : C. pH = 11.5
3. NH4Clના જલીય દ્રાવણની pH કેટલી હશે?
A. pH = 7
B. pH > 7
C. pH < 7
D. pH = 0
ઉત્તર : C. pH < 7
4. નીચેના પૈકી કયો ઍસિડ પ્રબળ છે ?
A. ઍસિટિક ઍસિડ
B. સાઇટ્રિક ઍસિડ
C. ઑક્ઝેલિક ઍસિડ
D. નાઇટ્રિક ઍસિડ
ઉત્તર : D. નાઇટ્રિક ઍસિડ
5. જો જલીય દ્રાવણો A, B, C અને Dની pH અનુક્રમે 1.9, 2.5, 2.1 અને 3.0 હોય, તો ઍસિડિકતાનો ક્રમ શું થશે?
A. A < C < B < D
B. D < C < B < A
C. D < B < C < A
D. D > C > B > A
ઉત્તર : C. D < B < C < A
6. કયું દ્રાવણ તટસ્થ સ્વભાવ ધરાવે છે?
A. ખાટાં ફળોનો રસ
B. લીંબુનો રસ
C. ધોવાના સોડાનું દ્રાવણ
D. મીઠાનું જલીય દ્રાવણ
ઉત્તર : D. મીઠાનું જલીય દ્રાવણ
7. જલીય દ્રાવણમાં ભૂરું લિટમસપત્ર નાખતા લાલ બને, તો તે દ્રાવણનું pH મૂલ્ય કેટલું હોય?
A. 0થી 7 વચ્ચે
B. 7થી 14 વચ્ચે
C. 14
D. 0
ઉત્તર : A. 0થી 7 વચ્ચે
8. દાંતનું બહારનું પડ શાનું બનેલું છે?
A. કૅલ્શિયમ ફૉસ્ફેટ
B. કૅલ્શિયમ નાઇટ્રેટ
C. પોટૅશિયમ ફૉસ્ફેટ
D. સોડિયમ ફૉસ્ફેટ
ઉત્તર : A. કૅલ્શિયમ ફૉસ્ફેટ
9. કયા ક્ષારના જલીય દ્રાવણની pH 7 હોય છે?
A. Na2CO3
B. CH3COONa
C. NH4Cl
D. KNO3
ઉત્તર : D. KNO3
10. CaCl2 + x → CaSO4 + 2NaClમાં x = ……..
A. Na2SO4
B. CaSO3
C. Na2SO3
D. CaSO2
ઉત્તર : A. Na2SO4
11. નીચેના પૈકી કઈ જોડ યોગ્ય નથી?
A. ખાટાં ફળો – સાઇટ્રિક ઍસિડ
B. દહીં – હૅક્ટિક ઍસિડ
C. કીડીનો ડંખ – મિથેનોઇક ઍસિડ
D. ટામેટાં – ટાર્ટરિક ઍસિડ
ઉત્તર : D. ટામેટાં – ટાર્ટરિક ઍસિડ
12. નીચેના પૈકી ક્યા ક્ષારના જલીય દ્રાવણમાં OH– આયનોનું પ્રમાણ વધારે હશે?
A. NaCl
B. Na2SO4
C. CH3COONa
D. બધામાં સમાન
ઉત્તર : C. CH3COONa
13. નીચેના પૈકી કયો પદાર્થ મંદ ઍસિડ સાથે પ્રક્રિયા કરી કાર્બન ડાયૉક્સાઇડ આપતો નથી?
A. માર્બલ
B. ચૂનાનો પથ્થર
C. ચૂનો
D. ખાવાનો સોડા
ઉત્તર : C. ચૂનો
મૂલ્યો આધારિત પ્રશ્નોત્તર (Value Based Questions with Answers)
1. રમેશના બાપુજી એક ખેડૂત છે. તેઓ તેમના ખેતરની જમીનમાં કોઈ પણ પાક ઉગાડી ના શકતા હોવાથી નિરાશ છે, કારણ કે તેમની જમીન વધુ પડતી બેઝિક હતી. આ થવાનું કારણ નજીકમાં સ્થપાયેલ કાગળ ઉદ્યોગનું નકામું પ્રવાહી કૅનાલમાં ઠલવાતું હતું, જે પાણી ખેતરની જમીનમાં વહન પામે છે. રમેશે ગામના અન્ય યુવકો સાથે મળીને કાગળ ઉદ્યોગના માલિકને તેમના દ્વારા થતા પ્રદૂષણની જાણ કરી.
(1) પાકના યોગ્ય વિકાસ માટે કેવા પ્રકારની જમીન હોવી જોઈએ?
(2) ખાતરોનો ઉપયોગ જમીનની pH માં બદલાવ લાવે છે. ખેડૂતો કેવી રીતે આ સમસ્યા ઉકેલે છે?
(3) ઉપરોક્ત ઉદાહરણમાં રમેશના કયા ગુણનું પ્રતિબિંબ પડે છે?
ઉત્તર :
(1) ખેતરની જમીન વધુ પડતી ઍસિડિક અથવા બેઝિક ના હોવી જોઈએ. એટલે કે પાકના વિકાસ માટે જમીન તટસ્થ હોવી જોઈએ.
(2) જો જમીન વધુ પડતી ઍસિડિક હોય, તો તેમાં ચૂનો ઉમેરીને જમીનને તટસ્થ કરવી જોઈએ અને જો બેઝિક હોય, તો તેમાં ઍસિડિક ક્ષારો ઉમેરીને જમીનને તટસ્થ કરવી જોઈએ.
(3) રમેશના જવાબદાર જાગૃત નાગરિક તરીકે અને સમૂહકાર્ય જેવા ગુણોનું પ્રતિબિંબ પડે છે.
2. રીટાની માતાને જ્યારે મધમાખીએ હાથમાં ડંખ માર્યો ત્યારે સખત દુખાવો થતો હતો. રીટાના દાદીએ દર્દમાંથી છુટકારો મળે તે માટે ડંખવાળા વિસ્તારમાં લોખંડ ઘસ્યું. પરંતુ રીટાએ રસોડામાંથી ખાવાનો સોડા લઈને ડંખવાળા હાથ પર ઘસ્યો. જેથી ઝડપથી દુખાવામાં રાહત મળી.
(1) મધમાખી કરડવાથી શા માટે દુખાવો થાય છે?
(2) ખાવાનો સોડા મધમાખીના ડંખના દુખાવાને કઈ રીતે દૂર કરે છે?
(3) ઉ૫૨ની ઘટનામાં રીટાનો કયો ગુણ દેખાય છે?
ઉત્તર :
(1) મધમાખીનો ડંખ ઍસિડ ધરાવે છે, જે શરીરમાં મુક્ત થતાં દુખાવો અને બળતરા થાય છે.
(2) ખાવાના સોડાનો સ્વભાવ બેઝિક છે. તે મધમાખીના ડંખ દ્વારા શરીરમાં મુક્ત થયેલ ઍસિડનું તટસ્થીકરણ કરે છે. પરિણામે દુખાવો દૂર થાય છે.
(3) રીટાના ત્વરિત, ચોક્કસ અને જવાબદાર વર્તણૂક જેવા ગુણ દેખાય છે.
3. ભરતનો મિત્ર જયદીપ કૉફીનો શોખ ધરાવે છે. તે દરરોજ સવારે શાળામાં બે કપ કૉફી પીવે છે અને અવારનવાર પેટના દુખાવાની ફરિયાદ કરે છે. ભરતે તેને સવા૨માં કૉફી ના પીવાની સલાહ આપે છે.
(1) પેટમાં દુખાવાનું કારણ શું છે?
(2) કૉફી પીધા પછી પેટમાંના પાચક રસોની pH કેટલી થશે?
(3) આ કાર્યમાં ભરતનો કયો ગુણ પ્રદર્શિત થાય છે?
ઉત્તર :
(1) કૉફી ઍસિડિટી કરે છે, જે અંતે પેટના દુખાવામાં પરિણમે છે.
(2) કૉફી પીધા પછી પેટના પાચક રસોની pH5 થાય છે.
(3) ભરતના કાળજી, લગાવ અને જાગૃતિના ગુણ પ્રદર્શિત થાય છે.
4. આશિષે નોંધ્યું કે, તેનો મિત્ર ટિફિનમાં કાયમ મીઠાઈ લાવે છે. જેના લીધે તેના દાંતમાં સડો થાય છે. આશિષે તેના મિત્રને સૂચન કર્યું છે કે તે શાળાના સમય દરમિયાન મીઠાઈ ઓછી ખાય, જેથી દાંતનો સડો અટકાવી શકાય.
(1) મીઠાઈ ખાવાથી દાંતમાં શા માટે સડો થાય છે?
(2) મીઠાઈ ખાધા પછી મુખની pH કેટલી થાય છે?
(3) આ કાર્યમાં આશિષનો કયો ગુણ દેખાય છે?
ઉત્તર :
(1) મીઠાઈ ખાવાથી મીઠાઈના કણો દાંતની અંદરની બાજુએ ચોંટી જાય છે. મીઠાઈના કણો પર બૅક્ટેરિયા ઉછરે છે અને ઍસિડ ઉત્પન્ન થાય છે, જેથી દાંતમાં સડો થાય છે.
(2) મીઠાઈ ખાધા પછી મુખની pH 2થી 6ના ગાળામાં રહે છે.
(3) આશિષના મિત્રતામાં નિષ્ઠા, જવાબદારી અને કાળજી રાખવાનો ગુણ દેખાય છે.
પ્રાયોગિક કૌશલ્યો આધારિત પ્રશ્નોત્તર (Practical Skill Based Questions with Answers)
1. પ્રયોગશાળામાં કસનળીનો ઘોડો મૂકેલો છે. સનળીઓમાં થોડોક ઍસિડ ભરેલો છે. આ ઍસિડોનું વર્ગીકરણ કેવી રીતે કરશો?
ઉત્તર : ઍસિડનું વર્ગીકરણ કરવા માટે આપણે ઍસિડની pH ચકાસવી જોઈએ અને તેમને પ્રબળ અથવા નિર્બળ ઍસિડમાં વર્ગીકૃત કરવા જોઈએ.
2. પાણીની pH શું છે? તે પાણીને ગરમ કરતાં pHમાં શું ફેરફાર થશે? શા માટે?
ઉત્તર : સામાન્ય રીતે શુદ્ધ પાણીની pHનું મૂલ્ય 25 °C તાપમાને 7.0 હોય છે. પાણીને ગરમ કરતાં તેનું pH મૂલ્ય બદલાય છે, કારણ કે પાણીને ગરમ કરતાં તેનું વધુ H+(aq) આયનમાં આયનીકરણ થતાં H+(aq)ની સાંદ્રતા વધતાં pH મૂલ્ય ઘટે છે.
3. પ્રયોગશાળામાં જુદાં જુદાં ઠંડાં પીણાંઓની pH શોધવા માટે કસોટી યોજવામાં આવી. અવલોકન કોઠો દોરી, પ્રયોગની એકઠી કરેલ માહિતી આપો. પરિણામનું પ્રાકથન કરો.
ઉત્તર : એકઠી કરેલ માહિતીનો અવલોકન કોઠો :
| ક્રમ |
પીણાં 1ની 7 pH |
પીણાં 2ની pH |
પીણાં 3ની pH |
|
1.
2.
3.
|
|
|
|
પ્રાથન : ઘેરા ઠંડા પીણાંની pHનું મૂલ્ય ઊંચું હશે. જે વધુ પડતું કૅફિન ધરાવે છે. જે વધુ ઍસિડિક છે અને ઠંડા પીણાં ઉઘાડતાં જે વધુ પરપોટા મુક્ત કરે છે. તે વધુ પડતા ઍસિડિક છે. જેમાં કાર્બોનેટેડ પાણી હાજર છે. તેની PH વધુ હશે.
हमसे जुड़ें, हमें फॉलो करे ..